- 1. Global byrde af livmoderhalskræft og screeningsudfordringer
Livmoderhalskræft er fortsat en stor global folkesundhedsudfordring, på trods af at den i vid udstrækning kan forebygges gennem effektiv screening og tidlig intervention. Ifølge Verdenssundhedsorganisationen (WHO) forekom der anslået 662.000 nye tilfælde og 349.000 dødsfald på verdensplan i 2022, hvilket rangerer den som den fjerde mest almindelige kræftform og den fjerde hyppigste årsag til kræftrelateret dødelighed blandt kvinder. Sygdomsbyrden er uforholdsmæssigt koncentreret i lav- og mellemindkomstlande (LMIC'er), hvor incidens- og dødelighedsraterne er betydeligt højere end i højindkomstlande. De skyldes primært manglen på screeningsprogrammer af høj kvalitet og effektiv påvisning og behandling af præcancerøse læsioner, forværret af:
-Manglende eller svag screeningsinfrastrukturMangel på tilgængelige, kvalitetssikrede screeningstjenester.
-RessourcebegrænsningerBegrænset laboratorieinfrastruktur, kølekædelogistik og pålidelig elektricitet.
-Mangel på arbejdskraftMangel på uddannet laboratorie- og klinisk personale.
-Forsinkelser og tab af opfølgningForsinkelse mellem prøveindsamling og tilgængeligheden af resultater, hvilket fører til forsinkelser i klinisk behandling eller tab af patienter til opfølgning[1].
2. Ætiologi og molekylært grundlag for cervikal karcinogenese
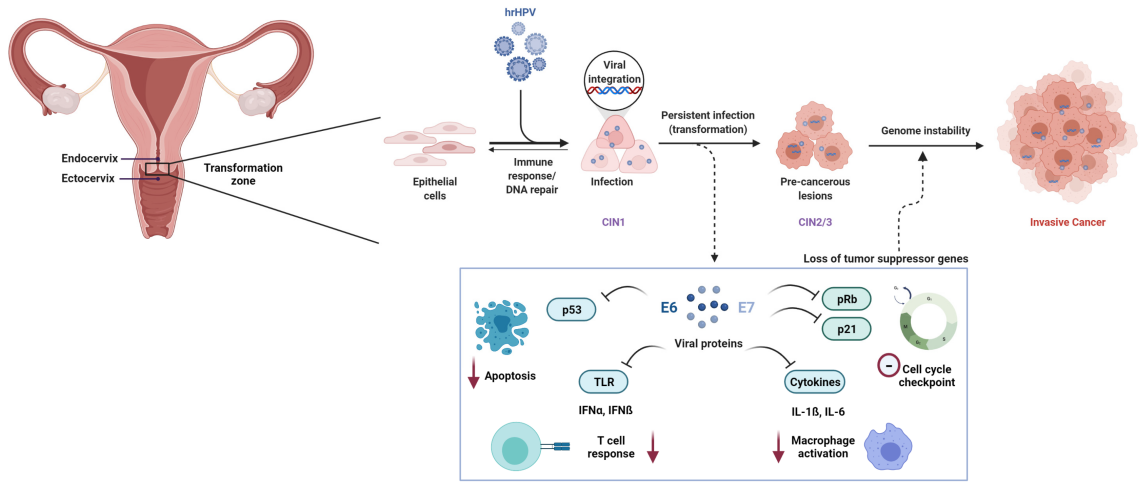
Vedvarende infektion med højrisiko human papillomavirus (HR-HPV) er en nødvendig årsag til livmoderhalskræft. Blandt mere end 200 identificerede HPV-genotyper er mindst12 typerer blevet klassificeret som kræftfremkaldende (gruppe 1) af Det Internationale Agentur for Kræftforskning (IARC).

På molekylært niveau er HPV-medieret carcinogenese primært drevet af de virale onkoproteiner E6 og E7. E6 fremmer nedbrydningen af tumorsuppressorproteinet p53, mens E7 funktionelt inaktiverer retinoblastomproteinet (Rb), hvilket resulterer i dysregulering af cellecyklussen og malign transformation.
3.WHO-anbefalede screeningsstrategier
Verdenssundhedsorganisationen anbefaler HPV-nukleinsyretest (NAT) som den foretrukne primære screeningsmetode til forebyggelse af livmoderhalskræft.
Den generelle befolkning:HPV DNA- eller mRNA-baserede NAT'er
Kvinder, der lever med HIV:HPV DNA-baserede NAT'er
Screeningsintervaller:
Kvinder i alderen 30-65 år: Hvert 5.-10. år
Kvinder, der lever med HIV: Hvert 3.-5. år
Sammenlignet med cytologibaserede metoder viser HPV-testninghøjere følsomhedog giveren overlegen negativ prædiktiv værdi, hvilket muliggør længere og mere omkostningseffektive screeningsintervaller.
4.WHO's målproduktprofil for HPV-screeningstests
WHO har udviklet enMålproduktprofil (TPP)til HPV-screeningsanalyser beregnet til brug i decentraliserede og ressourcebegrænsede miljøer.[1]
Nøgleegenskaber inkluderer:
- Kompatibilitet med selvindsamlede prøver
- Påvisning af flere højrisiko-HPV-genotyper (≥12 typer)
- Betjening af ikke-laboratorieuddannet personale
- Resultater tilgængelige inden for et enkelt klinisk møde
Disse kriterier understøtter point-of-care-testning og "screen-and-treat"-strategier.
5.En fuldt automatiseret platform til detektion af højrisiko-HPV
Macro & Micro-Tests AIO800-system levereren fuldt automatiseret arbejdsgang fra prøve til svarintegrering af nukleinsyreekstraktion, amplifikation og detektion i overensstemmelse med WHO-anbefalede screeningsstrategier.

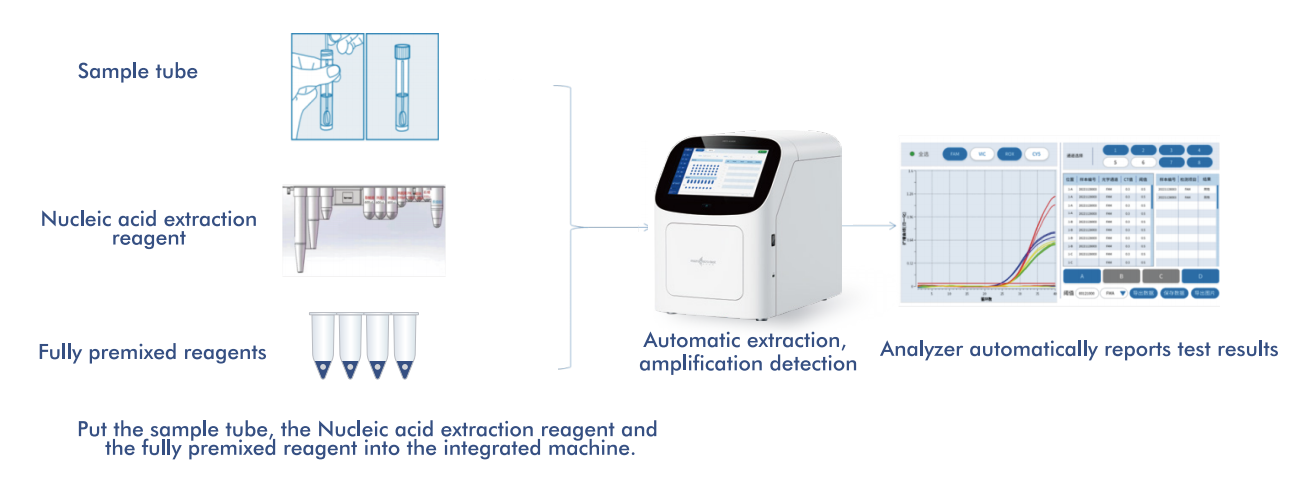
5.1 Automatiseret prøve-til-svar-workflow
Platformen integrerer ekstraktion, amplifikation og detektion af nukleinsyre i et enkelt, lukket system, der kræver minimal operatørindgriben. Dette design:
- -Reducerer afhængigheden af specialiseret laboratoriepersonale
- -Minimerer procesvariabilitet og kontamineringsrisiko
- -Muliggør implementering i decentraliserede sundhedsmiljøer
Samtidig understøtter dens gennemløbskapacitet anvendelse i centraliserede laboratorier, hvilket letter screeningsprogrammer i stor skala.
5.2 Bred genotypedækning
Systemet registrerer 14 højrisiko-HPV-typer, herunder alle 12 kræftfremkaldende typer klassificeret af IARC (HPV16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 og 59), samt HPV66 og HPV68.
Vigtigt er det, at det givertypespecifik genotypningresultater, hvilket muliggør risikostratificering og mere præcis klinisk behandling.
5.3 Analytisk sensitivitet og kliniske implikationer
Med en detektionsgrænse på 300 kopier/ml er systemet i stand til at identificere HPV-infektion på lavt niveau, der bidrager til:
- -Tidligere opdagelse af klinisk relevante infektioner
- -Forbedret negativ prædiktiv værdi
- -Understøttelse af forlængede screeningsintervaller
5.4 Understøttelse af selvprøvetagning
Platformen er kompatibel med beggepodningsprøver fra livmoderhalsen og selvudtagne urinprøveri overensstemmelse med WHO's anbefalinger for at håndtere centrale barrierer for screening, herunder:
- - Begrænset adgang til sundhedsfaciliteter
- -Sociokulturelle begrænsninger
Opslagstidspunkt: 27. marts 2026
