1 Baggrund for dengueepidemien: En eskalerende global folkesundhedsudfordring
Dengue er en akut myggebåren virussygdom forårsaget af denguevirus (DENV), som er blevet den hurtigst spredende arbovirussygdom globalt og udgør en betydelig trussel mod folkesundheden. I løbet af de sidste to årtier er den globale forekomst af dengue steget dramatisk, og antallet af rapporterede tilfælde er fordoblet årligt siden 2021 [1]. I december 2023 erklærede Verdenssundhedsorganisationen (WHO) en global dengue-nødsituation for at styrke den koordinerede internationale indsatser. Epidemiologiske estimater fra WHO viser, at cirka 3,9 milliarder individer verden over er i risiko for dengueinfektion, med anslået 390 millioner infektioner årligt - hvoraf 96 millioner præsenteres som klinisk tydelige tilfælde [1,2].
2 Epidemiologiske højdepunkter
De epidemiologiske karakteristika ved denguefeber er formet af samspillet mellem virologiske faktorer, vektorøkologi, værtens immunrespons og socio-miljømæssige forhold. En omfattende forståelse af disse karakteristika er afgørende for udviklingen af effektive forebyggelses- og kontrolstrategier samt præcise diagnostiske tilgange.
2.1 Transmissionsvektorer og bymæssige transmissionsmønstre
Denguevirus overføres primært viaAedes aegypti og Aedes albopictusmyg. Blandt disse vektorarter er Aedes aegypti anerkendt som den mest kritiske transmissionsvektor, karakteriseret ved høj "menneskelig tilpasningsevne" og udbredt udbredelse i tropiske og subtropiske bymiljøer. I modsætning til andre myggevektorer af arbovirale patogener udviser Aedes aegypti følgende vigtige epidemiologiske karakteristika:
- En præference for avl i menneskeskabte miljøer (f.eks. vandopbevaringsbeholdere, kasserede dæk)
-En stærk tropisme for menneskeblod som næringskilde
-Fødeadfærd om dagen
Disse træk definerer denguefeber som en typisk"byinfektionssygdom"med en betydeligt forhøjet transmissionseffektivitet i tætbefolkede områder. WHO-relaterede studier har vist, at i byområder med høj befolkningstæthed kan øget hyppighed af kontakt mellem myg og mennesker øge det grundlæggende reproduktionstal (R₀) for DENV betydeligt og derved accelerere spredningen af epidemier [2].
2.2 Globale spredningstendenser og drivende faktorer
Ifølge WHO-rapporter er det globale antal rapporterede denguetilfælde steget eksponentielt i løbet af de sidste to årtier [1,3]. Denne opadgående tendens er primært drevet af følgende sammenhængende faktorer:
(1) Klimaændringer: Stigende globale temperaturer udvider ikke blot det geografiske område af egnede levesteder for mygvektorer, men forkorter også den ydre inkubationsperiode for DENV i mygværten, hvilket forbedrer transmissionseffektiviteten. Klimainducerede variationer i mygtætheden er blevet valideret af WHO som en pålidelig indikator for den spatiotemporale dynamikker i dengueudbrud.
(2) Urbanisering: Hurtig og uplanlagt byudvidelse har skabt rigelige yngleområder for mygvektorer, mens øget befolkningstæthed har styrket kontinuiteten i DENV-smittekæderne.
(3) Global befolkningsbevægelse: International rejseaktivitet og handel har muliggjort hurtig grænseoverskridende transmission af DENV og fremmet overgangen fra importerede tilfælde til vedvarende lokal transmission. WHO's overvågningsdata viser, at USA mellem 2010 og 2021 rapporterede 7.528 rejserelaterede denguetilfælde, hvoraf 3.135 krævede hospitalsindlæggelse, og 19 resulterede i dødelighed.
(4) Udvidelse af vektordistribution: Globalt set fortsætter det geografiske udbredelsesområde for Aedes aegypti og Aedes albopictus med at udvide sig, og Aedes-myggene etablerer sig i stigende grad i dele af Europa. Som følge heraf har dengue udviklet sig fra en traditionelt regional epidemi til en global trussel mod folkesundheden.
2.3 Multiserotype-cocirkulation og reinfektionsmekanismer
Denguevirus omfatter fire antigenisk forskellige serotyper (DENV-1 til DENV-4). Infektion med én serotype giver langvarig beskyttende immunitet mod den specifikke serotype, men kun midlertidig og delvis krydsbeskyttelse mod de andre tre serotyper. Den generelle befolkning er universelt modtagelig for DENV, hvor kun en delmængde af inficerede individer udvikler klinisk sygdom [2].
I endemiske områder cirkulerer flere DENV-serotyper ofte samtidigt, hvilket resulterer i potentialet for, at individer oplever flere dengueinfektioner i løbet af deres liv. WHO's epidemiologiske undersøgelser har identificeret multi-serotype co-cirkulation som en nøglefaktor for periodiske dengueudbrud [1].
2.4 Sekundær infektion og antistofafhængig forstærkning
Et kritisk og unikt fænomen inden for dengueepidemiologi erantistofafhængig forstærkning (ADE)Under sekundær infektion med en heterolog DENV-serotype letter ikke-neutraliserende antistoffer produceret under den primære infektion virusindtrængen i monocytter og makrofager, hvorved virusreplikation forbedres. Denne mekanisme er bredt anerkendt af WHO som en væsentlig patogen faktor i alvorlig denguefeber, herunder dengue hæmoragisk feber og dengue shock syndrom [1].
WHO's epidemiologiske data viser konsekvent, at personer med sekundær dengueinfektion har en signifikant højere risiko for at udvikle alvorlig sygdom sammenlignet med personer med primær infektion – en egenskab, der er af stor betydning for sygdomsovervågning og klinisk behandling. Det er vigtigt at bemærke, at selvom risikoen for alvorlig sygdom er forhøjet under sekundær infektion, kan infektion med enhver DENV-serotype potentielt udvikle sig til alvorlig dengue [1].
2.5 Uspecifikke kliniske manifestationer og risiko for fejldiagnose
De kliniske manifestationer af denguefeber er markant uspecifikke, især i de tidlige stadier af sygdommen, og overlapper ofte med andre myggebårne virusinfektioner (f.eks. chikungunya- og Zika-virus) samt visse luftvejsinfektioner. WHO's estimater viser, at 40-80 % af DENV-infektioner er asymptomatiske [3].
Typiske kliniske manifestationer omfatter:
-Akut feber (vedvarer i 2-7 dage, kan være tofaset)
-Svær hovedpine og retroorbital smerte (smerter bag øjnene)
- Muskel- og ledsmerter (almindeligvis omtalt som "knoglebrudsfeber")
-Makulært eller makulopapulært udslæt
-Mild blødning (f.eks. ekkymose, epistaxis, tandkødsblødning)
Symptomatisk denguefeber opdeles typisk i tre forskellige faser: feberfasen, den kritiske fase og helbredelsesfasen. Cirka mindre end 5% af symptomatiske patienter udvikler svær denguefeber. På grund af manglen på specifikke kliniske træk er diagnose baseret udelukkende på kliniske symptomer udfordrende, hvilket øger risikoen for fejldiagnose og underdiagnose. WHO understreger eksplicit, at klinisk diagnose alene er utilstrækkelig til at sikre nøjagtighed, hvilket gør laboratoriebekræftelse uundværlig [1].
3 nøglepunkter fra WHO “Laboratorietestning for denguevirus: Midlertidig vejledning, april 2025”
I april 2025 udgav Verdenssundhedsorganisationen (WHO) opdaterede, midlertidige retningslinjer for laboratorietestning af DENV, som giver autoritativ teknisk vejledning til global denguediagnose. Denne vejledning sammenfatter den seneste evidens om laboratorietestning af denguefeber i forbindelse med den igangværende globale dengue-krise og tilbyder praktiske anbefalinger, der er skræddersyet til miljøer med varierende ressourceniveauer.

3.1 Grundlæggende principper for teststrategi
Vejledningen understreger, at diagnosen af denguefeber skal baseres på en kombineret teststrategi med flere markører baseret på sygdommens stadium [1]. I mangel af en universel diagnostisk algoritme bør teststrategierne tilpasses lokale epidemiologiske kontekster under hensyntagen til følgende nøglefaktorer [1]:
-Infektionsstadium: Antallet af dage efter symptomdebut bestemmer den mest passende testmetode.
-Prøvetype: Egnetheden af fuldblod, plasma eller serum til DENV-detektion
-Regional epidemiologi: De lokalt cirkulerende DENV-serotyper og co-cirkulation af andre arbovirusser
-Risiko for samtidig infektion: I regioner med overlappende arboviruscirkulation bør multiplex-testning overvejes for at skelne mellem forskellige patogener.
3.2 Fasebaseret teststrategi
Ifølge WHO's retningslinjer bør laboratorietest for denguefeber følge klare tidsvinduer baseret på sygdommens stadium [1,2]:
(1) Akutfasetestning (≤7 dage efter debut)
-Nukleinsyretestning (molekylær testning): Omvendt transkription-polymerasekædereaktion (RT-PCR) og andre molekylære metoder detekterer DENV RNA med høj følsomhed.
-Antigentestning: NS1-antigendetektion, som bliver detekterbar inden for 1-3 dage efter debut.
I den akutte fase er viræminiveauerne relativt høje, og testning af nukleinsyre og antigen opnår optimal følsomhed.
(2) Testning i rekonvalescensfasen (≥4 dage efter debut)
-Serologisk testning: IgM-antistoffer kan typisk detekteres omkring dag 4 efter debut.
-I de fleste tilfælde varer IgM-antistoffer i 14-20 dage, og i nogle tilfælde kan persistensen vare op til 90 dage.
-IgG-testning har begrænset værdi til diagnose af akut denguefeber på grund af potentielle krydsreaktive antistoffer fra tidligere flavivirusinfektion eller vaccination.
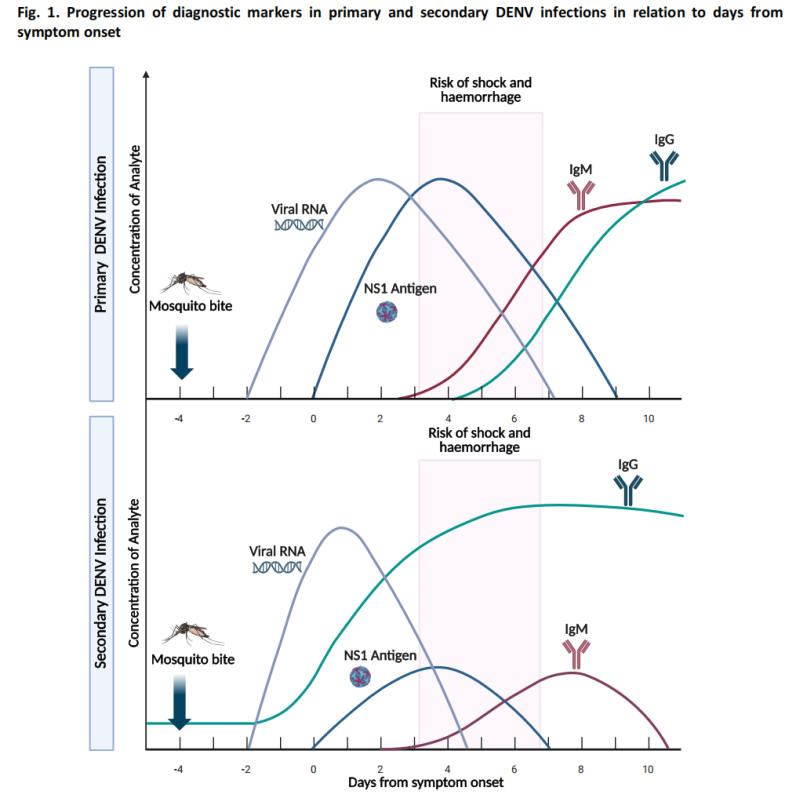
(3) Algoritme til diagnosticering af mistænkte tilfælde
Vejledningen indeholder en diagnostisk algoritme til mistænkte tilfælde af denguefeber og anbefaler passende testmetoder baseret på dage efter symptomdebut: NS1-antigentest og nukleinsyretest er de primære tilgange i den tidlige fase, mens serologisk test er den primære metode i den senere fase.
3.3 Evaluering og udvælgelse af testmetoders ydeevne
Ifølge WHO er en systematisk evaluering af ydeevnen og anvendelige scenarier for forskellige denguetestninger som følger:
| Testmetode | Mål | Tidsvindue | Primært applikationsscenarie | Overvejelser |
| Nukleinsyretestning | Viralt RNA | 1-7 dage efter debut | Tidlig bekræftelse, serotypeidentifikation | Guldstandardmetode; kræver specialiseret laboratorieudstyr og teknisk ekspertise |
| NS1-antigentestning | Ikke-strukturelt protein | 1-3 dage efter debut | Tidlig hurtig screening | Fås i hurtig diagnostisk test (RDT) format, egnet til ressourcebegrænsede miljøer |
| IgM-antistoftestning | Specifikke IgM-antistoffer | ≥4 dage efter debut | Diagnose af nylig infektion | En enkelt serumprøve antyder kun en mulig nylig infektion; serokonversion er nødvendig for bekræftelse |
| IgG-antistoftestning | Specifikke IgG-antistoffer | Rekonvalescerende/tidligere infektion | Epidemiologisk undersøgelse, vurdering af immunitetsstatus | En enkelt serumprøve er ikke egnet til diagnose af akut denguefeber |
| Kombineret testning (NS1+IgM/IgG) | Antigen + Antistoffer | Fuldt sygdomsforløb | Omfattende diagnose af dengueinfektion | I øjeblikket det bedst fungerende RDT-format til denguediagnose |
| NGS | Viralt RNA | 1-7 dage efter debut | Viral genomisk overvågning | Kræver specialiseret sekventeringsudstyr og bioinformatiske analysefunktioner |
4 Makro- og mikrotest-produktanbefalinger til denguedetektion efter scenarie
For at understøtte forebyggelse og bekæmpelse af denguefeber tilbyder Macro & Micro-Test en integreret diagnostisk portefølje, der dækker hurtig screening, molekylær bekræftelse og genomisk overvågning, og som opfylder behov på tværs af forskellige faser af udbrudshåndtering.
4.1 Scenarie 1: Hurtig screening og målrettet overvågning
Gælder for feberklinikker, primære sundhedsfaciliteter, screening for udbrud i lokalsamfundet og karantæne i havne/på grænsen.
-Denguevirus NS1-antigenhurtigtest: Opdager tidlig infektion (1-3 dage efter debut) med resultater inden for 15 minutter til hurtig triage.
-Denguevirus IgM/IgG-antistoftest: Skelner mellem primære/sekundære infektioner for at evaluere risikoen for alvorlig sygdom.
-Denguevirus NS1 Antigen + IgM/IgG Kombineret Hurtigtest: Detekterer antigen og antistoffer samtidigt til fuld diagnose.
-Chikungunya-virus IgM/IgG-antistoftest: Muliggør differentialdiagnose med denguefeber for præcis identifikation af patogener.
4.2 Scenarie 2: Præcisionsdiagnose og nødberedskab
-Denguevirus I/II/III/IV Nukleinsyredetektionskit: Detekterer og differentierer 4 serotyper (detektionsgrænse 500 kopier/ml) til sporing af udbrud.
-Lyofiliseret denguevirus PCR-kit: Kan transporteres ved stuetemperatur, egnet til ressourcebegrænsede områder og pludselige udbrud.
-Dengue/Zika/Chikungunya Multiplex Real-Time PCR Kit: Detekterer 3 arbovirusser samtidigt for effektiv differentialdiagnose ved komplekse udbrud.

Alle ovenstående reagenser er kompatible med AIO 800 Fully Automated Sample-to-Answer System, hvilket reducerer manuel betjening og krydskontaminering og forbedrer effektivitet og biosikkerhed.
4.3 Scenarie 3: Genomisk overvågning og analyse af viral afstamning
Gælder for nationale referencelaboratorier og forskningsinstitutioner inden for folkesundhed, i overensstemmelse med WHO's positionering af NGS.
Macro & Micro-Tests genomiske overvågningsløsninger understøtter helgenomsekventering til virussporing, afklaring af transmissionskæden, variantovervågning og justering af vaccinestrategi. De understøtter manuelle/automatiserede arbejdsgange, hvilket forbedrer gennemløb og reproducerbarhed og gør det muligt for laboratorier at opgradere fra rutinemæssig testning til avanceret overvågning, hvilket er i overensstemmelse med WHO's vægtning af at styrke overvågningen af viral evolution.

4.4 Værdi af integrerede løsninger
Macro & Micro-Test leverer komplette diagnostiske løsninger til påvisning af arbovirus, der understøtter hvert trin i udbrudshåndteringen: hurtige screeningsværktøjer til frontlinjesundhedsmiljøer, molekylær bekræftelse til præcis diagnose og helgenomanalysefunktioner til epidemiologisk overvågning. Med højtydende assays, fleksible arbejdsgange og automatiseringsklare platforme giver disse løsninger laboratorier og folkesundhedssystemer mulighed for at styrke beredskabet og reaktionen på nye arbovirustrusler verden over.
Referencer
[1] Verdenssundhedsorganisationen. Laboratorietestning for denguevirus: Midlertidig vejledning, april 2025. Genève: Verdenssundhedsorganisationen; 2025.
[2] WHO's tekniske rådgivningsgruppe for det globale arbovirusinitiativ. Styrkelse af det globale beredskab og den globale reaktion på trusler fra arbovirussygdomme: En opfordring til handling. Lancet Infect Dis. 2026;26(1):15-17.
[3] Lancet-mikroben. Overvindelse af dilemmaet ved denguediagnostik. Lancet Microbe. 2025;6(7):101190.
Opslagstidspunkt: 20. marts 2026
